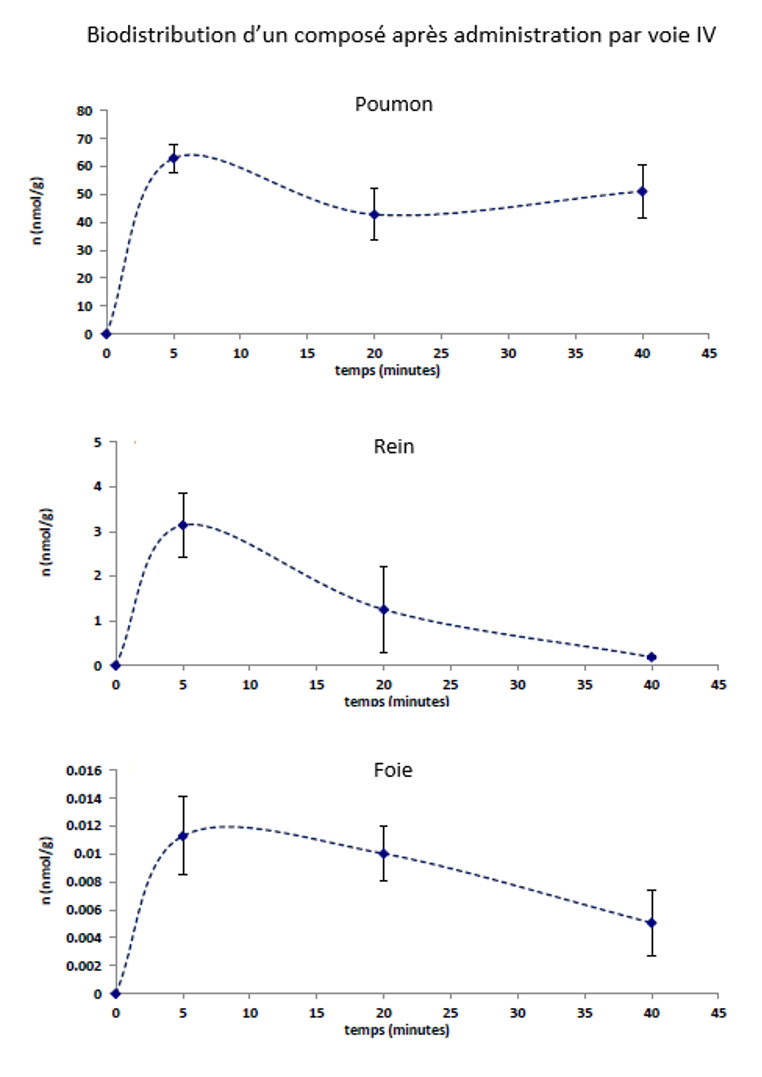
La biodistribution est l’étude du devenir d’un candidat médicament dans l’organisme par l’analyse de l’évolution de ses concentrations dans le/les organe(s) cibles au cours du temps. Elle dépend des caractéristiques physicochimiques du candidat médicament, de son absorption dans le sang, de la vascularisation de la/les cible(s), de sa distribution et de sa rétention dans le/les organe(s) et de l’intégrité des barrières biologiques (paroi vasculaire, barrière hématoencéphalique…)
La biodistribution du composé depuis le sang vers les tissus cibles pour son activité principale ou vers d’autres tissus ou organes, pouvant entraîner l’apparition d’effets indésirables, peut-être mesurée chez des animaux sains ou dans les modèles pathologiques.
Il est en effet démontré qu’une pathologie peut modifier l’intégrité et/ou la perméabilité des barrières biologiques et peut donc influencer l’ADME d’un composé (Absorption, Distribution, Métabolisation et Élimination)
Exemples :
- une inflammation locale augmentera la perméabilité des capillaires sanguin et augmentera la disponibilité d’un composé sur le site inflammatoire.
- Une tumeur dans un organe sera également plus accessible du fait de l’augmentation de la vascularisation.
- Le passage de la BHE ( ou BBB : « Blood brain barrier ») est aussi fortement influencé en présence d’une pathologie.
- Une atteinte de la fonction rénale ou hépatique peut réduire l’élimination d’un candidat-médicament et augmenter son efficacité biologique et/ou ses effets indésirables…
Déterminer la biodistribution d’une composé dans le modèle pathologique est donc d’un grand intérêt.
Aucun modèle standard ne peut préjuger de cette biodistribution dans la pathologie étudiée.
Il est donc indispensable de la réaliser dans le même modèle que celui utilisé pour étudier l’efficacité thérapeutique du candidat-médicament.
Le modèle peut-être reproduit mais cela demande généralement une mise au point lourde et une formation externe pour valider les compétences requises.
Pour ces raisons, nous proposons de réaliser la biodistribution dans vos modèles, maitrisés et réalisés par vos équipes.
Il est alors possible :
- d’effectuer le transfert des animaux vers notre service de zootechnie
- de nous déplacer dans votre établissement afin de réaliser les prélèvements dans les meilleurs conditions et selon nos standard.
La biodistribution d’un médicament déterminent son efficacité thérapeutique, ses effets secondaires et sa toxicité.
Les paramètres mesurés lors d’une étude de biodistribution:
– Concentration maximale du principe actif dans le/les organe(s) d’intérêt(s) (C max)
– Temps nécessaire au principe actif pour atteindre la concentration C max (T max)
– Demie vie (temps qui permet de réduire de 50% la concentration maximale du principe actif)
Il est également possible d’étudier les métabolites lorsqu’ils ont été préalablement identifiés.